| К. К. ГЕДРОЙЦ | ХИМИЧЕСКИЙ АНАЛИЗ ПОЧВ |
Щелочность водных вытяжек из почвы обусловливается присутствием в них карбонатов щелочных и щелочно-земельных металлов и щелочных солей кремневой и органических кислот; для определения щелочности, вызываемой в отдельности каждой из этих групп солей, не существует методов; можно определять только общую щелочность, вызываемую совокупностью этих соединений; вообще говоря, в большинстве почв эта общая щелочность вызывается главным образом карбонатами. Но общую щелочность почвы можно расчленить, с одной стороны, на щелочность, вызываемую нормальными карбонатами (углекислыми щелочами, преимущественно Na2CO3; сюда же войдет, по всей вероятности, щелочность, вызываемая щелочными солями органических и кремневой кислот), и на щелочность, вызываемую всеми двуглесолями; а с другой стороны, на щелочность, вызываемую углесолями щелочных металлов (сюда же войдет, по всей вероятности, щелочность, вызываемая щелочными солями кремневой и органических кислот), и на щелочность, вызываемую щелочноземельными карбонатами.
По ходу анализа удобнее начинять с определения щелочности, вызываемой нормальными карбонатами.
Определение щелочности, вызываемой нормальными карбонатами, или количества иона СО3. К 25-50 к. стм. водной вытяжки в небольшом стаканчике прибавляют 1-2 капли фенол-фталеина 1); если жидкость окрасилась в красный цвет, то это признак присутствия в ней нормальных карбонатов; в этом случае жидкость титруют 0,01 или 0,02 нормальной серной или соляной кислотой до исчезновения окраски, для большей точности определения конца титрования следует рядом со стаканчиком, в котором производится титрование, поставить такой же величины другой стаканчик с таким же количеством той же вытяжки; оба стаканчика должны стоять на листе белой бумаги; в стаканчик, в который прибавлен фенолфталеин, приливают по каплям титрованную кислоту до тех пор, пока окраска жидкости в нем не сравняется с окраской жидкости в стаканчике, не содержащем фенол-фталеина.
1) Приготовление индикатора: 1 гр. фенол-фталеина растворяют в 100 к. стм. 96% алкоголя.
Так как розовая окраска от фенол-фталеина исчезает тогда, когда весь нормальный карбонат перейдет в двууглекислый согласно уравнению: 2 Na2CO3 + H2SO4 = 2 NaHCO3 + Na2SO4, то число к. стм. истраченной кислоты (m), умноженное на 2, т.-е. 2m, будет соответствовать количеству нормального карбоната. Само собою разумеется, что если предполагается производить определение количества нормальных карбонатов, то необходимо для приготовления вытяжки применять воду, лишенную углекислоты.
Определение общей щелочности. В тот же стаканчик с водной вытяжкой от предыдущего определения после прибавления к ней фенол-фталеина, если в вытяжке не оказалось нормального карбоната, или после окончания вышеописанного титрования, если в вытяжке таковой оказался, прибавляют одну - две капли метил-оранжа 1) и продолжают титровать той же кислотой до появления розовой окраски. Как и в предыдущем случае, титрование необходимо вести при наличности другого стаканчика, такого же диаметра с таким же количеством вытяжки и таким же количеством метил-оранжа; оба стаканчика должны стоять на листе белой бумаги; оттенки в жидкостях обоих стаканов до титрования должны быть одинаковы; при титровании нужно сравнивать между собой цвет жидкости в обоих стаканах, и как только оттенок в стакане, в который приливается кислота, изменится по сравнению с оттенком в другом стакане, слегка порозовеет, титрование окончено; при некотором навыке легко улавливается малейшее изменение в оттенке.
Все количество кислоты, пошедшее на титрование в присутствии фенол-фталеина и метил-оранжа, будет соответствовать общей щелочности взятого количества водной вытяжки; обозначим это количество кислоты через n.
1) Приготовление индикатора: 0,05 гр. метил-оранжа растворяют в 100 к. стм. воды.
Определение щелочности, вызываемой углекислыми щелочами. Для этого определения необходимо выделить из водной вытяжки углекислый кальций. По нашим данным, наилучший результат дает следующий способ.
50 к. стм. вытяжки выпаривается досуха на водяной бане в небольшой платиновой чашечке; не давая чашке остыть, обрабатывают содержимое возможно меньшими порциями горячей воды, не содержащей углекислоты, при помощи стеклянной палочки с каучуковым наконечником, и фильтруют каждый раз раствор через маленький фильтр (7 стм. в диаметре) в стаканчик; для полного растворения щелочных карбонатов и промывания чашки вполне достаточно 10 порций воды; кроме того еще ополаскивают два раза фильтр. Чем меньше будет употреблено воды и чем быстрее будет окончено растворение (быстро фильтрующая воронка и хорошо прилаженный фильтр), тем полнее будет отделение щелочных карбонатов от щелочноземельных. Если вытяжка содержит сравнительно много последних, что будет видно по осадку на фильтре, то собранный фильтрат следует вторично выпарить и т. д. Иногда при фильтрации получается мутный фильтрат; в таких случаях приходится выпаривать новое количество вытяжки и фильтровать через плотный фильтр; титровать с мутью же ни в каком случае не следует, так как в ней могут содержаться щелочноземельные карбонаты. Полученный фильтрат, содержащий щелочные углесоли, как нормальные, так и двууглекислые, по охлаждении титруется в присутствии метил-оранжа 0,01 или 0,02 норм. кислотой совершенно так же, как при предыдущем определении, до появления розового оттенка; пусть при этом титровании пойдет р к. стм. 0,01 или 0,02 нормальной кислоты. Тогда на основании трех полученных данных (2m, n, р) производят расчет для взятого количества вытяжки по следующей схеме:
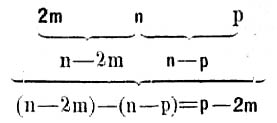
Примечание 1. Определение щелочности представляет особый интерес в солонцах и вообще солонцеватых почвах (т. е. в почвах или в горизонтах почвы, содержащих в поглощающем комплексе натрий). Но здесь особенно необходимо иметь ввиду условность получаемых результатов, их зависимость от продолжительности и способа хранения образцов в лаборатории, от соотношения между почвой и водой при приготовлении водных вытяжек, от времени взаимодействия между почвою и водою (вытяжки из солонцов фильтруются очень медленно и неодинаково медленно у различных солонцев, а этот промежуток времени может столько отразиться на щелочности). Особенно сильно все это сказывается в тех солонцах, в которых содержатся щелочно-земельные карбонаты и где поэтому при взаимодействии между почвою и водою идет усиленный обмен цеолитного (и гуматного) натрия на щелочно-земельные металлы карбонатов с образованием соды; здесь, напр., более продолжительная фильтрация вытяжки сейчас же отражается повышением содержания соды, так как, вследствие доступа углекислоты воздуха, вместо прореагировавшего с почвою двууглекислого кальция получается в растворе новое его количество, а значит и новое количество соды и т. д.
Примечание 2. Вытяжки из солонцеватых почв часто бывают очень интенсивно окрашенными гуматами; для определения щелочности приходится тогда брать малые количества и разбавлять их для титрования водою. Общую щелочность, Са (НСО3) и NaHCO3 можно в этом случае определять, выпаривши вытяжку и прокаливши остаток; при этом только необходимо иметь ввиду, что при таком ходе анализа определяется и вся та сода, которая должна возникнуть из натрия, связанного с гу-матами и кремнекислотой, находящимися в вытяжке. Такое определение во всяком случае может представлять интерес и помимо выше описанного.